Cofepris emite alerta por medicamentos para el cáncer y VIH falsificados
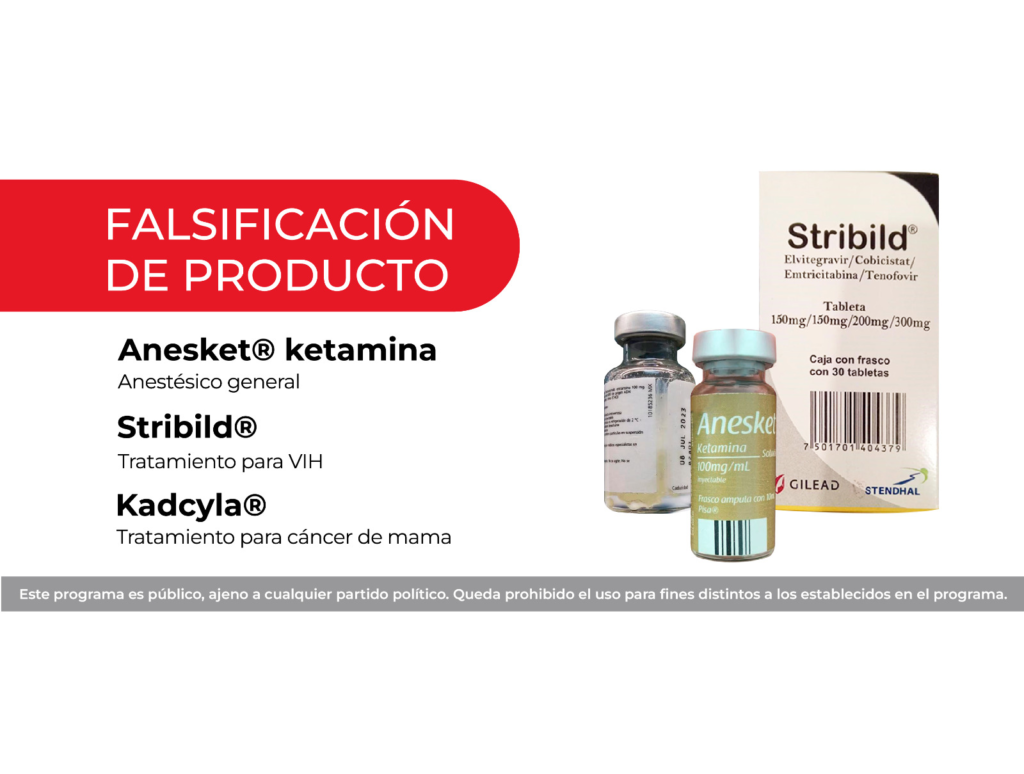
La Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) emitió una alerta por la falsificación de tres medicamentos: Kadcyla, para pacientes con cáncer de mama; Stribild, un tratamiento para VIH, y Anesket Ketamina, un anestésico general.
La empresa Productos Roche informó que los lotes B2801 –con caducidad 8 de julio 2023– y el lote B1019 –fecha de vencimiento 20 de abril 2023–, ambos del producto Kadcyla (trastuzumab emtansina), en presentación frasco de 100 mg, son falsos.
La autoridad señaló que una de las irregularidades presentes en estos medicamentos apócrifos es el código 10185236 MX, que se localiza en la parte superior de la etiqueta; además, el líquido presenta coloración amarillenta al momento de su preparación.
Cofepris señaló que el producto Stribild (elvitegravir, cobicistat, emtricitabina, tenofovir), con lote ZBXB, muestra las fechas de caducidad 25 de noviembre 2023 y 25 de febrero 2025, las cuales son falsas. Además, la empresa titular del registro sanitario solicitó a Cofepris la revocación del registro sanitario en noviembre de 2020, por lo que la comercialización de esos lotes es ilegal, sin importar la fecha de caducidad.
La autoridad sanitaria también señaló la falsificación del anestésico Anesket ketamina frasco ámpula de 50mg/mL, con lote C21G904, de la cual se detectó que la fecha de caducidad no pertenece a la autorizada en el registro sanitario; además, la tipografía e impresión no corresponden al producto original. Asimismo, la presentación de 100 mg/mL, lote 2113470 y caducidad 11-2026 no se encuentra autorizada, por lo que se determinó su irregularidad.
La Comisión recomendó no adquirir ninguno de los productos con las características citadas, ya que al ser irregulares no se garantiza su seguridad, calidad y eficacia y representan un riesgo para la salud, pues se desconocen las condiciones de fabricación, almacenamiento y distribución, así como el origen de sus ingredientes.
En caso de presentar cualquier reacción adversa o malestar por el suministro de estos productos, la Cofepris puso a disposición el siguiente correo electrónico para levantar el reporte correspondiente: farmacovigilancia@cofepris.gob.mx
Con información de PROCESO.
